台灣微脂體申請經濟部A+企業創新研發淬鍊計畫-快速審查臨床試驗計畫「新劑型新藥Prodex(TLC399)第一/二期臨床試驗計畫」,業經經濟部審查通過並簽訂專案契約書。該計畫全程開發期程36個月,補助經費為新台幣1759萬元,占計畫經費39%。
2015/01/07經濟日報/記者黃文奇/台北報導
我們一般對新藥開發的印象其實是『新成分新藥』(NCE) 的開發模式,其實還有很多類別可以合法的說自己是『新藥』,而您知道您投資的新藥是屬於哪種新藥嗎?影響是甚麼?究竟新聞中指出的「新劑型新藥」是什麼呢?
製藥產業
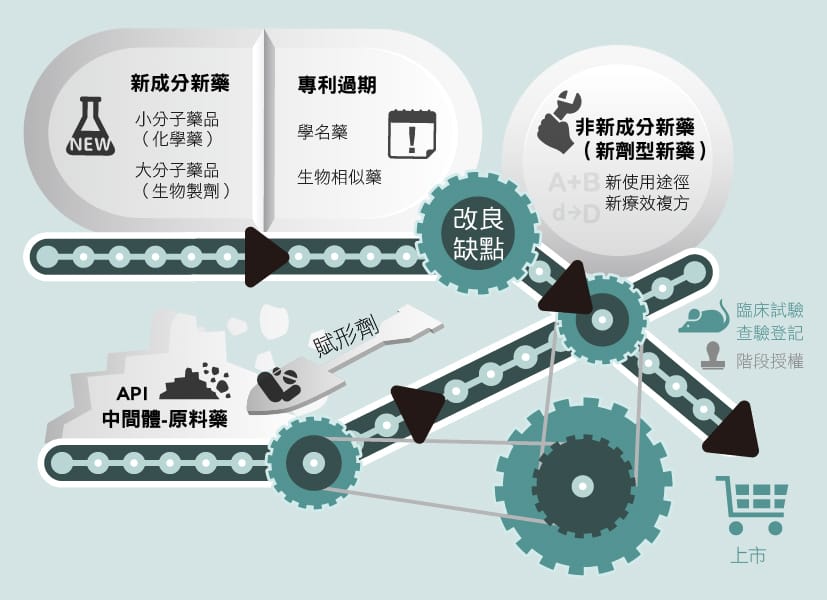
在台灣所定義的藥物開發市場中,除了萬眾矚目的新成分新藥(NCE,New Chemical Entity ),其實還有其他類別的研發也算是新藥−具備新療效複方或是新使用途徑的藥品,以及性質與新藥相近而被列入新藥:新劑型、新使用劑量、新單位含量之製劑。其他這幾類可歸類為非新成分新藥(非NCE)。
新成分新藥(NCE)開發是一條漫長的路,不僅耗時花錢,更有可能竹籃子打水一場空,投入的風險極大,相較之下,以已上市的藥品為基礎去改良,藥品安全性已經過驗證,臨床試驗所花費的時間及成本皆較小,成功上市的機會較大。
新成分新藥(NCE)
新成分的發現到最後藥品的成功上市,必須經過複雜冗長的藥物探索期、動物試驗、臨床試驗和主管單位核准的過程,歷時12至15年不等,耗費資金高達150~200億台幣,且8,000~10,000 個化合物中只有1個化合物最終可獲批准上市。
非新成分新藥(非NCE)
簡略而言係利用藥物傳輸技術,改良現有藥物之缺點,提高藥效、降低副作用、以及擴大臨床應用等,讓已有的藥物已以新面貌再次申請新藥上市,降低新藥研發之經費並縮短時程。欲發展非新成分新藥,必須對於藥物傳遞系統有深入了解及掌握關鍵技術,才能讓產品具有獨特性和市場價值。
台微體(4152-TW)在產業中的商機
台灣微脂體主要專注於藥物傳輸系統的研發,利用專利或特殊藥物傳輸系統降低毒性、改善藥效,繼而發展成特殊學名藥、新劑型/新配方藥物及新藥。目前已成功開發台灣第一個微脂體抗癌藥物力得(Lipo-Dox),獲台灣衛生署許可證核准上市,並於2002 年3 月獲得健保給付,銷售據點分布亞洲各國及全台四十餘點,主要客戶為各大醫學中心腫瘤科;目前原廠藥已退出台灣市場,力得(Lipo-Dox)市佔率達100%;全身性黴菌感染特殊學名藥安畢黴(AmBiL),獲台灣衛生署許可證核准上市,並於2013 年7 月獲得健保以原廠藥同額給付,上市初期尚無市佔率資訊。另自2010 年起與國際藥廠運作授權合作開發模式,並於2014 年起與國際藥廠開啟技術相乘的合作開發模式。
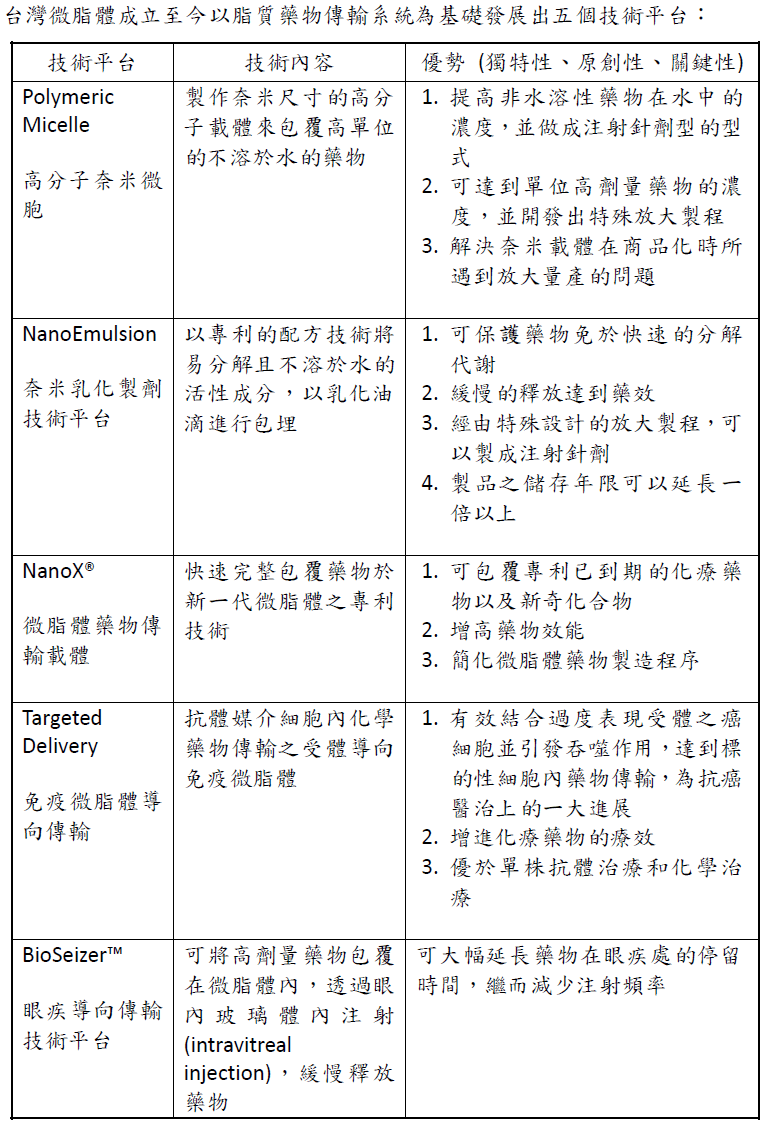
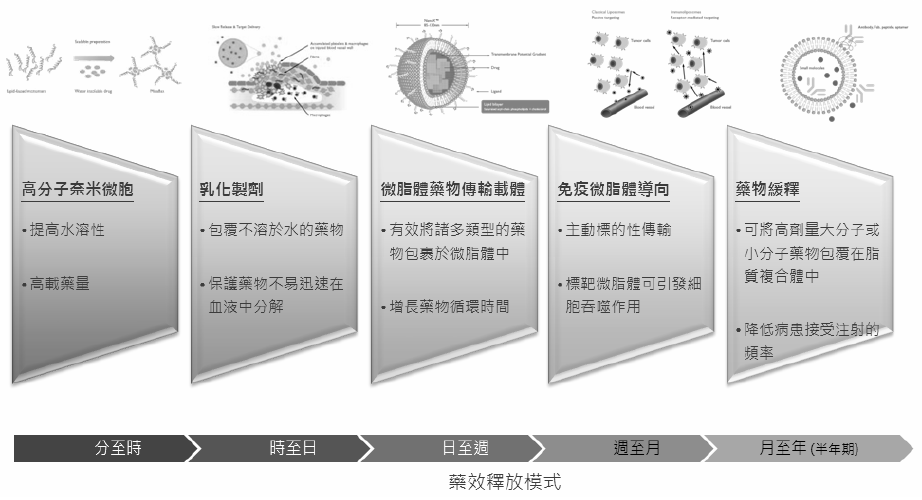
這些脂質傳輸系統讓台灣微脂體得以跳脫單純研發微脂體技術的公司,而晉升成為一家專業的藥物傳輸系統設計暨新藥開發公司。
公司登記之所營事業如下:
一、F108021 西藥批發業。
二、F107070 動物用藥品批發業。
三、F107080 環境用藥批發業。
四、F108031 醫療器材批發業。
五、F208021 西藥零售業。
六、F207070 動物用藥零售業。
七、F207080 環境用藥零售業。
八、F208031 醫療器材零售業。
九、F401010 國際貿易業。
十、F203010 食品、飲料零售業。
十一、F601010 智慧財產權業。
十二、I103010 企業經營管理顧問業。
十三、I103030 醫院管理顧問業。
十四、IC01010 藥品檢驗業。|
十五、IG01010 生物技術服務業。
十六、ZZ99999 除許可業務外,得經營法令非禁止或限制之業務
產品研究發展現況
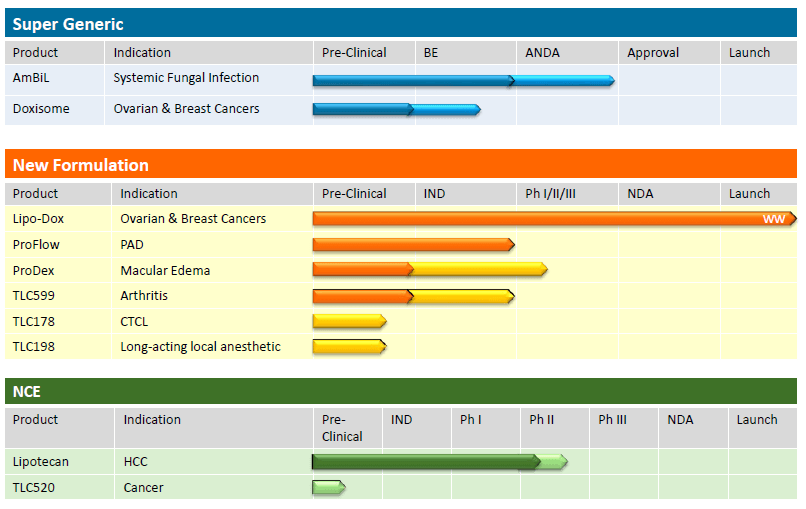
資料來源:台微體法說會
主要商品(服務)銷售地區
全球主要的醫藥市場分別有其特性,也因此雖然疾病無國界,但適合各醫藥市場的產品仍依其屬性不同而有所區別。以歐美市場為例,由於市場規模大且生活水準較高,除了資源較充沛外,人民的知識也普遍性較高,因此對於新藥的接受度相較於亞洲地區高,因此歐美藥廠均傾向於投資風險較高但報酬也相對可觀的新藥。反觀亞洲以及其他Pharmerging 市場,由於許多仍為成長中國家,在資源較少且病患所能獲知的醫藥訊息較不透明的情況下,當地藥廠對於學名藥的接受度比較高。
有鑑於各別市場特性不同的情況下,台灣微脂體旗下產品的目標市場也各有異:新藥與新劑型/新配方藥物如Lipotecan、ProDex、TLC599、TLC198、TLC178等的主要銷售市場為美國與歐洲;而如ProFlow 將主要銷售至亞洲醫藥市場;AmBiL 與Doxisome 等特殊學名藥則可於全世界行銷。如此一來,台灣微脂體方可將有限的事業開發人力運用至最適合各產品的市場,獲得事半功倍之效。
產業之現況與發展
A.國外市場:
a. 製藥產業持續成長:
根據IMS 統計分析,全球生技製藥產業於2013 年產值為9,890 億美金,相較於2008 年的7,950 億美金增加1,940 億,五年增幅24.4%,複合式成長率5.2%。預估未來在2014-2018 年期間,複合式成長率約4~7%,與過去五年期間2009-2013 的相比,增長加速的可能性極大。
b. Pharmerging 國家成長迅速
以市場的產值分佈而言,北美仍以37%位居全球之冠,與歐洲(24%)及亞洲(29%)共據90%的全球市場。歐洲的成長率為1~4%,美國的成長率達5~8%,全球的複合成長率達4~7%。而當主要生技製藥市場的成長率趨緩時,包含中國大陸在內的17 個「pharmerging」國家(Pharmerging 國家意指製藥業日漸重視的發展中國家,包含阿根廷、巴西、中國大陸、埃及、印度、印尼、墨西哥、巴基斯坦、波蘭、羅馬尼亞、俄羅斯、南非、泰國、土耳其、烏克蘭、委內瑞拉與越南等十七個國家。)的成長率估計將有8~11%之譜,在2013年有2,500 億美金的規模。中國大陸在2013 年躍升成為全球第二大市場,將會在2018 達到1,700 億美金的規模。
c.新藥研發費用劇增
就市場未來發展趨勢而言,儘管研發費用逐年遞增,但通過藥證審核、實際可上市的藥物並未隨之增加。自1990-2010 年以來,大型藥廠所花費的總研發費已達每藥證平均2,558 億美金。但每年取得藥證的數量卻始終維持在20 餘例之譜,以至於兩者之間產生越來越大的差距 (Innovation Gap),大幅影響藥廠的利潤。
d.原廠藥專利到期
此外,這些國際藥廠所持有的原廠藥諸多將面臨專利到期的問題。一但原廠藥失去專利的保護,學名藥業者便會迅速推出價格約原廠藥1/5 的學名藥,原廠藥也將面臨市占率的迅速流失以及利潤的大幅壓縮,估計於2012-2016 年間這些國際知名的藥廠將因旗下明星藥物的專利屆期而損失近1,270 億美金的營收,約占現今市場規模的13%。
e.學名藥市場蓬勃發展
另一方面,原廠藥的專利過期,對於製藥廠商來說雖是相當大的打擊,但對於學名藥市場來說,卻意味著蓬勃的發展。除了專利到期之外,各國政府方面也因為面臨全球人口老年化導致醫療費用逐年攀升的財務窘境,而先後立法鼓勵學名藥的使用,促進了學名藥市場超過2018 年全球成長市值的52%。
B.國內市場:
根據經濟部生技產業白皮書針對從事生技相關的廠商所進行的調查顯示,2013 年我國生技產業產值約為新台幣2,769 億元,較2012 年成長5%。從次領域的產值分佈來看,醫療器材產值比重是最高(42%);生技藥品產值成長為6%,預期未來我國生技產業仍將保持成長等於全球複合式成長率5.3%。
目前國內業界投入癌症新藥研發之公司,除了本公司外,另有基亞(3176-TW)公司、台灣東洋(4105-TW)公司、太景生技公司與智擎(4162-TW)公司,預期未來新藥開發仍有其利基空間,累計至2014 年4 月止,有70 家審定為生技新藥公司,審定為生技新藥的品項共計163 項,惟其新藥開發技術層面進入門檻高,處方開發、放大研究與法規規範會是挑戰,但可預期的是國內應會有更多新藥開發經驗累積。
產業上、中、下游之關聯性
台微體之行業上、中、下游之關聯性如上圖所示,包括國內外之前臨床及臨床試驗中心、原料藥及藥品代工廠、醫藥公司及行銷通路等,由於前期研發費時且不確定性高,因而採用合作研發模式,增加產品開發來源,以自有評估系統降低開發風險,同時與上下游建立為長期緊密合作的伙伴關係,使研發成果價值化,發揮最大效益。
長期業務發展計畫
台灣微脂體公司之理想是為台灣生技製藥產業植入最新國際研發模式,利用藥物傳輸技術,改良現有藥物之缺點,提高藥效、降低副作用、以及擴大臨床應用等,以降低新藥研發之經費並縮短時程,同時提供病患更安全的治療與更優質的生活品質;此外,於藥物開發研究過程與臨床醫師共同合作,針對國際藥廠較少投入之華人特殊疾病進行治療研究,為疾病治療帶來貢獻。
目前全世界專注於脂質載體技術研發之公司屈指可數,雖然國際大藥廠皆有投入微脂體研發,但專業資源與技術的不足也常導致研發失敗,部分大藥廠則以委託研究、併購或技術移轉方式尋求新產品來源。因此,若能建立一專業脂質載體技術研發公司,擁有最先進之技術,即能具備長期發展潛力;對台灣生技製藥產業而言,除可促進產業研究發展外,對於整體產業的國際競爭力提升,也會有很大助益。在此背景下,台灣微脂體公司之願景,即為建立一『立足台灣,放眼全球的生技製藥領導者』。
A.行銷業務方面
(A)掌握歐美主流市場
(B)積極拓展新興國家市場,建立緊密的行銷網。支援重點客戶,配合公司資源,追求公司最大利潤。
B.研發方面
(A)開發癌症、眼疾、麻醉、關節炎及老化相關疾病新劑型新藥及新藥,擴充完整產品線。
(B)發展基因治療、長效釋放及標靶治療新藥。
C.生產方面:
(A)建立精實的供應鏈及作業流程,因應中長期市場結構與企業策略的改變。
(B)建立自有之生產廠,因應產品線擴充之需求。
D.營運及財務方面:
(A)積極朝全球國際化佈局發展,培養國際化人才,使營運規模及觸角持續穩定擴大,以成為世界級公司。
(B)以一系列的產品線佈局,取得穩定收入來源,作為公司營業規模快速提升之資本後援,以降低經營成本,並減少經營風險。
大事件紀錄
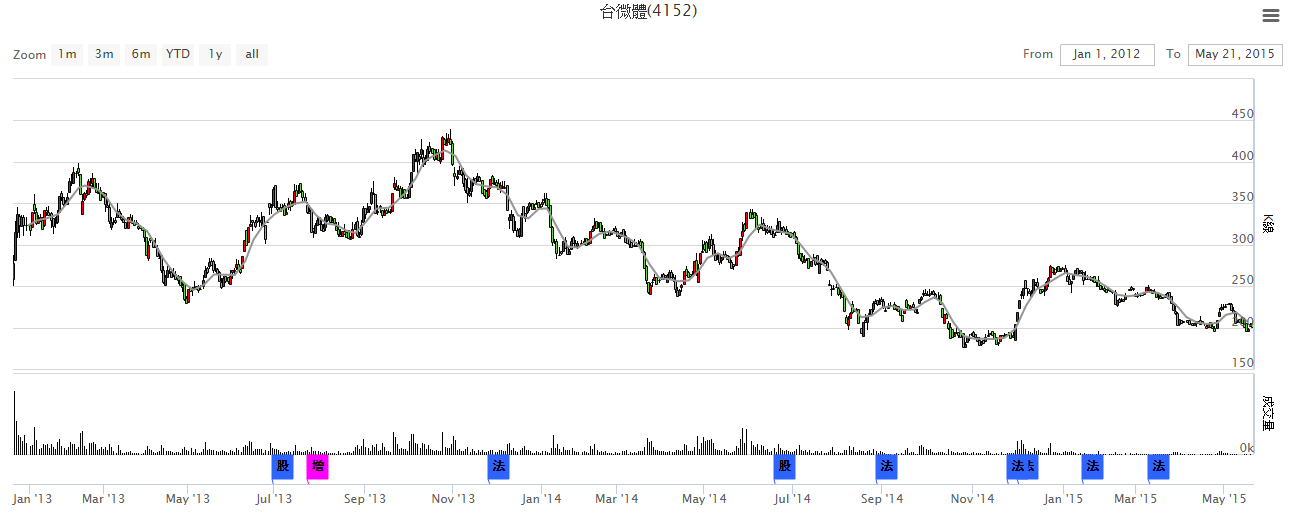
資料來源:股狗網
2012/3/24
本公司(台微體)與TEVA PHARMACEUTICALS (“TEVA”)及安成國 際藥業股份有限公司(“安成”)簽訂藥品開發與銷售合約
2012/12/21
台微體21日158元上櫃
2012/12/22
新藥指標股王的台微體21日掛牌,股價果然不負眾望,終場大漲120元以278元收盤、漲幅高達75.95%,並爆出4,026張大量,單日即吸金逾10億元,高佔上櫃總成交值的一成
2013/2/6
全球市場大缺貨用於治療卵巢癌及乳癌的Doxil,4日由印度藥廠Sun Pharma領先台微體取得第1張學名藥證,將搶攻全球6億美元市場下,導致台微體、安成(4180)慘遭空頭襲擊,股價重挫。
2013/2/28
研發全身性黴菌感染之特殊學名藥AmBiL,與永信(3705-TW)簽訂台灣區銷售合約
2013/3/13
於公開說明書記載 Lipotecan已於美國及歐洲取得原發性肝癌孤兒藥候選藥物認証,適用於原發性肝癌、腎細胞癌,產品開發進度已進入第二期臨床試驗。
2013/4/2
一向為多頭指標的生醫股,昨(1)日在市場傳言股市聞人林滄海賣股、個股去年度財報不佳、籌碼凌亂和停損賣壓等多項利空夾擊,股價重挫,新藥股首當其衝,台微體收跌停價287.5元,跌破日前暫訂的現增承銷價298元;基亞、智擎、美時(1795)等跌幅都逾6%。
2013/5/5
生醫股遭空襲 募資現陰霾:就統計來看,9家辦理增資的公司,除了龍燈(4141-TW)已進入繳款作業、預計在5月7日完成現增案外;包括台微體、中天(4128-TW)的現增案都被要求補件,而二家公司也分別於4/19和4/15日完成補正送件,如果未再被要求補件,預計20個營業日生效,5月中旬即可明朗。
被視為是新藥股指標的台微體,這次規劃辦理1,000萬股現增案,每股溢價原訂298元,預計募資20億元,在這一波的生醫股募資潮中居冠;不過,該股卻因增資案遭主管機關質疑,導致股價下修,從歷史天價回檔至3日的244元,跌幅高達38%,預計若現增案過關,每股溢價勢必要調降。
2013/6/2
台微體受惠抗癌新藥Lipotecan(立普帝康),取得中國食品藥品監督管理局特殊審批,加上入選MSCI成份股,上周五股價上漲2.67%,以269元收盤,技術面已突破壓力區,在打底完成後,若後市量能放大,可視為多頭攻擊訊號。
2013/6/26
研發以週邊血管疾病為適應症之新劑型/新配方藥物ProFlow,與國際藥廠SciClone簽訂合作開發架構協議,授權其於中國及港、澳之銷售權利。此次簽約,SciClone將依里程碑支付總額美元3,950萬元予本公司分期入帳,包含簽約金150萬元、以及研發里程款、銷售里程款等。
2013/7/2
新藥公司台灣微脂體昨(1)日宣布,公司自行研發針對「全身性黴菌感染症」的特殊學名藥安畢黴(AmBiL),正式取得衛生署審定通過國產藥品「安畢黴微脂粒凍晶注射劑50毫克」醫師指示藥品許可證。
2013/8/27
台灣微脂體昨(26)日宣布,公司與韓國藥廠SamChunDang(SCD)簽定抗感染藥物「安畢黴(AmBiL)」銷售授權協議,為該藥物首次跨出台灣,拿下亞洲第一個市場。
2013/8/27
研發全身性黴菌感染之特殊學名藥AmBiL,與SamChunDang Pharm Co.,Ltd.簽訂韓國藥品銷售合約
2013/12/19
台灣微脂體昨(18)日宣布,與國際學名藥大廠Sandoz AG(山德士)簽訂合作協議,並將其所研發抗黴菌藥物「AmBiL(安畢黴)」歐洲與美國的銷售事宜授權給Sandoz負責,搶攻4億美元(近新台幣120億元)市場。
2013/12/23
新劑型藥物ProDex取得美國食品藥物管理局核 可進行人體臨床試驗
2014/4/18
台微體攜外商 攻抗癌藥 與比利時藥廠Ablynx合作開發 最快明年動物試驗 後市看好
2014/9/16
台微體新癌藥 兩岸報捷 Lipotecan大進展 進入臨床二期試驗 搶攻亞洲生技商機
2014/9/25
台微體眼藥傳輸系統 獲美專利
2014/11/15
擴張全球版圖 台微體 澳洲設子公司
2014/12/6
九合一選舉結果從「藍天」變「綠地」,昨(1)日相關概念股股價兩樣情,金衛(910801)、永豐金(2890-TW)、大魯閣(1432)等「連陣營」概念股大跌,「柯P」因之前支持力挺生技,昨日生技股等表現相對強勢。
2015/1/7
申請經濟部A+企業創新研發淬鍊計畫-快速審查臨床試驗計畫「TLC399第一/二期臨床試驗計畫」,業經經濟部審查通過並簽訂專案契約書。
(1)該計畫全程開發期程36個月,計畫總經費新台幣4521萬元,補助經費為新台幣1759萬元,占計畫經費39%。
(2)補助經費將於未來依全程計畫書所定進度分期撥款。
2015/2/27
台微體去年每股虧11.54元
2015/4/11
「疏水性喜樹鹼衍生物之醫藥組合物」取得台 灣發明專利
2015/4/28
TLC599(關節炎新劑型藥物)取得台灣衛生福利部 食品藥物管理署核准進行人體臨床試驗
參考資料:
1.公開資訊觀測站
2.經濟日報
3.工商時報
4.台微體年報
5.台微體2015法說會
6.另闢蹊徑,新藥開發的另一片天空 http://goo.gl/5CYuLf
7.新藥密碼:505(b)(1)、(b) (2)、(j) http://goo.gl/Co30C8
§本網站個股介紹僅就公司在產業趨勢中的機會及年報、新聞的整理,真正的公司評價仍需從總體經濟、財務資訊或公司經營等全方面著手,本整理所提供的資訊僅供參考,也無任何推介買賣之意,所有資訊仍應以資料來源公告為準。











走過百年歷史的刮鬍刀老店吉列-它的護城河在哪裡-__-.png)









