因重倉特斯拉( Tesla, TSLA-US )而實現驚人業績的 ARK Investment Management 近日發布了 2021 年年度投資報告。由於其在科技領域卓越而長遠的眼界, ARK 的 Big Ideas 系列年度報告以往在專業金融圈被奉為科技投資 “ 聖經 ” 。在他們傳奇般的特斯拉戰績火遍全球之後,今年的年度報告更加引人矚目。
在今年的報告中, “ 新科股神 ” Cathie Wood 帶領她的 ARK 研究團隊提出了 15 個宏大而前景廣闊的投資主題,涉及的領域除了為人熟知的比特幣、電動車、無人駕駛之外,還包括深度學習、新一代基因測序、數據中心再創造、虛擬世界等。
在 ARK 看來,這些主題不僅僅是今年可以重點關注的主題,還在未來數年都擁有巨大的市場以及投資空間。比如,他們認為,深度學習將在未來 15 ~ 20 年裡為全球股票市場增加 30 兆美元的市值。此外,他們預計某些領域可能將要或者正在出現極具創新力的顛覆性進展。其中,比特幣可能迎來以機構作為投資主力的全新時代,數據中心產業正在經歷一場翻天覆地式的技術革命,數位錢包將從根本上撼動全世界傳統銀行的地位,而電動車的銷量將暴增 20 倍⋯⋯。
長讀測序(即第三代 DNA 測序)
長讀測序( Long-Read Sequencing,LRS ),即第三代 DNA 測序技術,可以繪製更加完整的人類基因組圖譜。
下一代 DNA 測序是基因組革命背後的驅動力。雖然短讀測序(Short-Read Sequencing,SRS)在過去占主導地位,但 ARK 認為,長讀測序將迅速獲取市場佔有率。
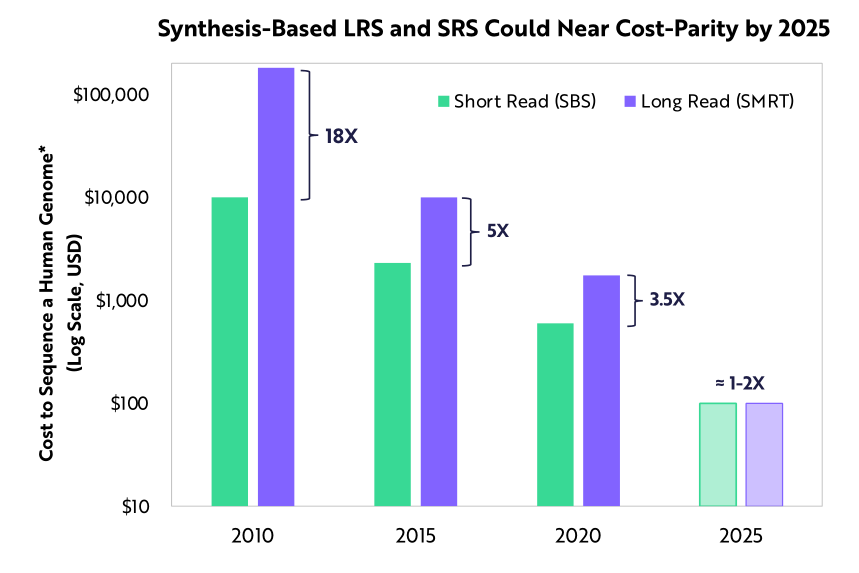
ARK 認為,與短讀測序相比,長讀測序技術可以提供更高的準確性、更全面的變體檢測以及更豐富的功能集。到 2025 年底,高精準度的長讀測序和短讀測序的成本將相近。我們預計,長讀測序市場規模將以每年 82 %的年化成長率擴張,從 2020 年的 2.5 億美元成長到 2025 年的 50 億美元左右。
基因組 “ 工具包 ” 正在擴展,以提供更完整、更豐富、更準確的生物學視圖
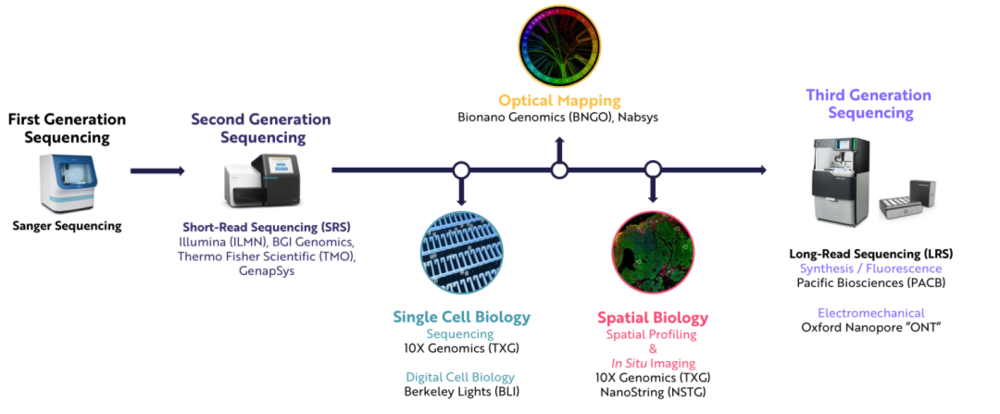
以往,研究人員不得不在短讀測序的準確性和長讀測序的全面性之間做出選擇。長讀測序和短讀測序系統都將基因組分解成較小的片段,都用高解析度光學元件掃描基因片段,並使用高性能電腦算法重組基因組。
短讀測序系統將許多小的( 150bp )片段混合到一個共有序列中。此方法可捕獲小的突變,但不能檢測到較大的基因重組(基因體結構變異)或隱藏在重複基因組區域中的突變。以往的長讀測序系統能夠讀取的基因較長(大於 10,000bp ),雖然測得的鹼基準確性較差,卻提供了更完整的基因組圖譜。
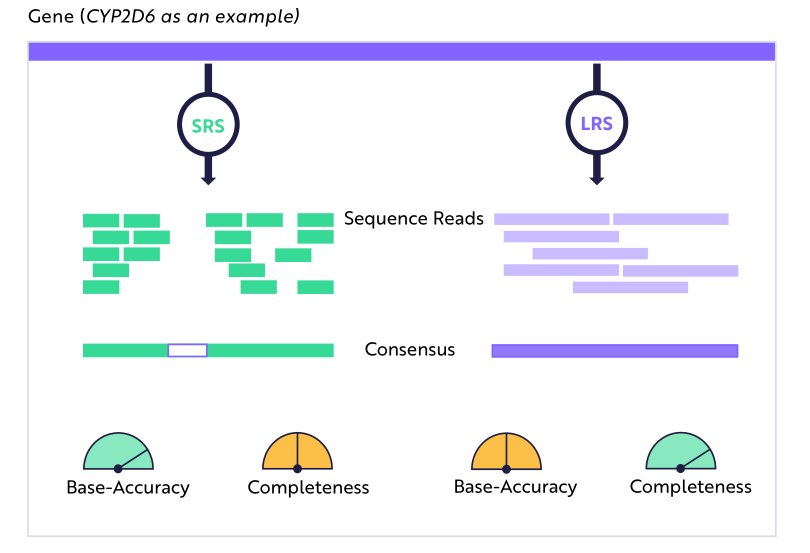
隨著長讀測序的成本趨近於短讀測序,許多臨床應用可能轉向長讀測序
借助 Google DeepVariant 等深度學習算法,無論是基於合成測序還是基於奈米孔測序的長讀測序方法都可以迅速提高性能。儘管目前基於奈米孔測序技術的長讀測序測得的鹼基準確性較差,但它可以以約 500 美元的價格產生整個人類基因組序列,比短讀測序具有更高的成本效益。儘管基於合成測序技術的長讀測序價格更高,但根據 PrecisionFDA Truth Challenge V2 獲得的結果,它的精度比短讀測序高 2.5 倍,比基於奈米孔測序技術的長讀測序高 30 倍。
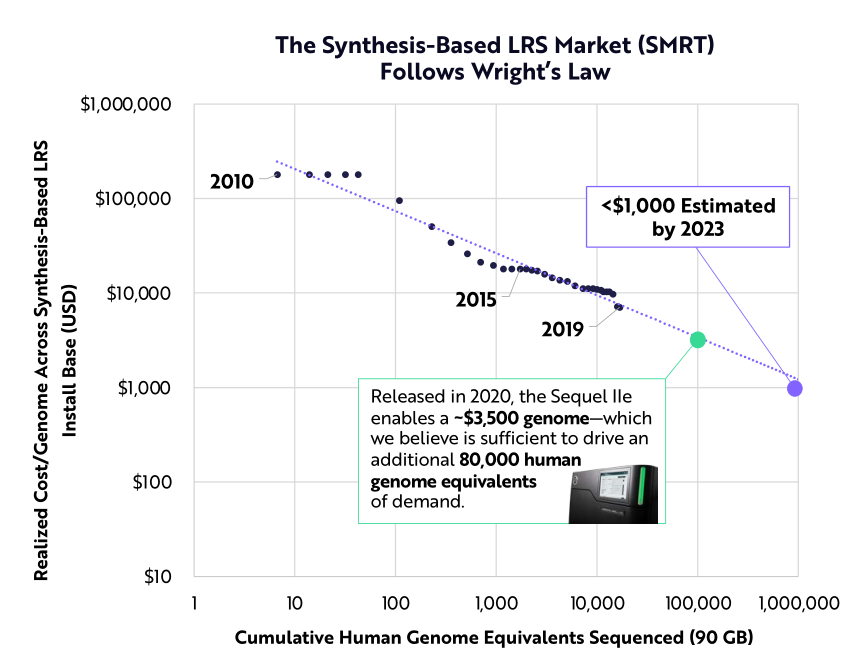
根據萊特定律,基於合成測序的長讀測序所產生的數據每累積增加一倍,其成本就會下降 28 %
長讀測序的獨特功能主要受成本和頻寬改進的推動。長讀測序不需要擴增,還可以天然進行甲基化檢測,並且可以跨越完整的RNA分子。ARK 估計,使用長讀測序技術對整個人類基因組進行測序的成本將降至 100 ~ 200 美元。到 2025 年底,該技術在所有變體類型的準確性都將優於短讀測序。
ARK 相信長讀測序分析在很多測序應用中都是領先的
某些臨床應用,如兒科重症監護環境下的快速全基因組測序( WGS ),報銷率很高,使得診斷提供商能夠更靈活性地改用長讀測序。無論是存在於容易測序還是難以測序的基因組區域中,大小不一的遺傳變體都會影響患者的表型。在 ARK 看來,無論序列如何,長讀測序工具都可以提供最全面的變體檢測。

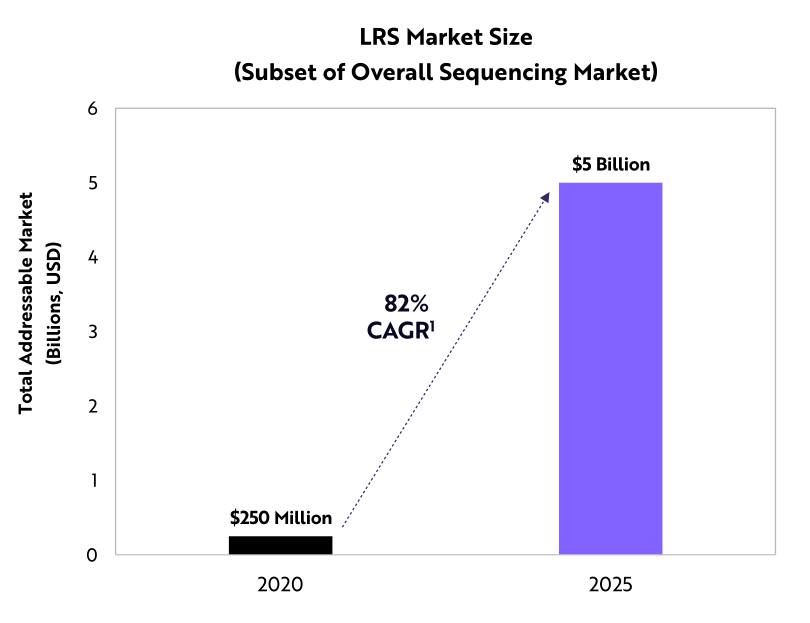
ARK 預計,到 2025 年,長讀測序市場將以每年 82 %的年化成長率擴張
ARK 認為,由於較低的測序成本以及對高精度和完整結果的需求,市場對長讀測序的需求正觸及拐點。包括測序耗材、儀器和服務在內,到 2025 年長讀測序的創收規模將從 2.5 億美元成長到 50 億美元。短讀測序將繼續主導測序市場,特別是隨著液體活檢成為腫瘤診療的標準。
多癌症篩查
液體活檢比以往任何醫學乾預都可預防因癌症而發生的死亡。
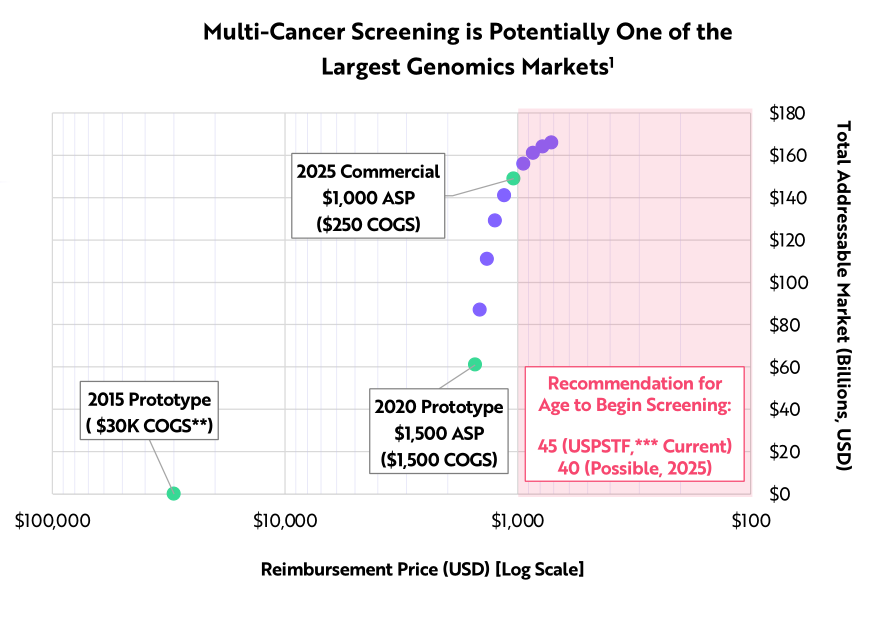
根據 ARK 的研究,通過結合多種創新技術,多癌症篩查的成本從 2015 年的 30,000 美元下降到如今的 1,500 美元,降低了 20 倍;預計到 2025 年再降低 80% 至 250 美元。
因此,美國多癌症篩查市場的規模將達到 1,500 億美元。據統計,一項多癌症篩查方案可以避免美國每年 66,000 例癌症死亡,挽救 140 萬人的生命。
早診斷,早治療,早康復
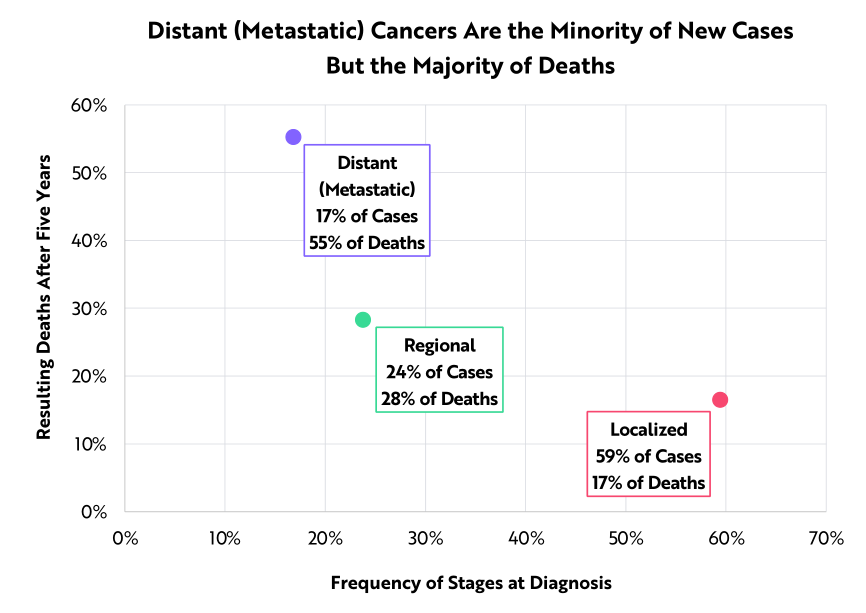
所有腫瘤都遵循從在原位發現、可治療,到病變發生轉移、不可治療的這種可預測的過程,這為早期檢測提供了依據。轉移性癌症僅佔新發病例的 17% ,但在 5 年的時間裡卻造成了 55% 的癌症死亡。原位癌的 5 年加權平均生存率為 89% ,而轉移癌的 5 年加權平均生存率僅為 24% 。
通過血液檢測,多種癌症篩查可以發現幾十種早期癌症
隨著體細胞突變、循環蛋白和免疫訊號的出現,機器學習算法已經將 DNA 甲基化作為一種新的、高度敏感的早期癌症檢測生物標誌物。下一代 DNA 測序的成本快速下降,使得液體活檢成為可能。合成生物學的發展正在幫助臨床醫生在高分貝噪聲環境(如血液)中發現微弱的癌症訊號。
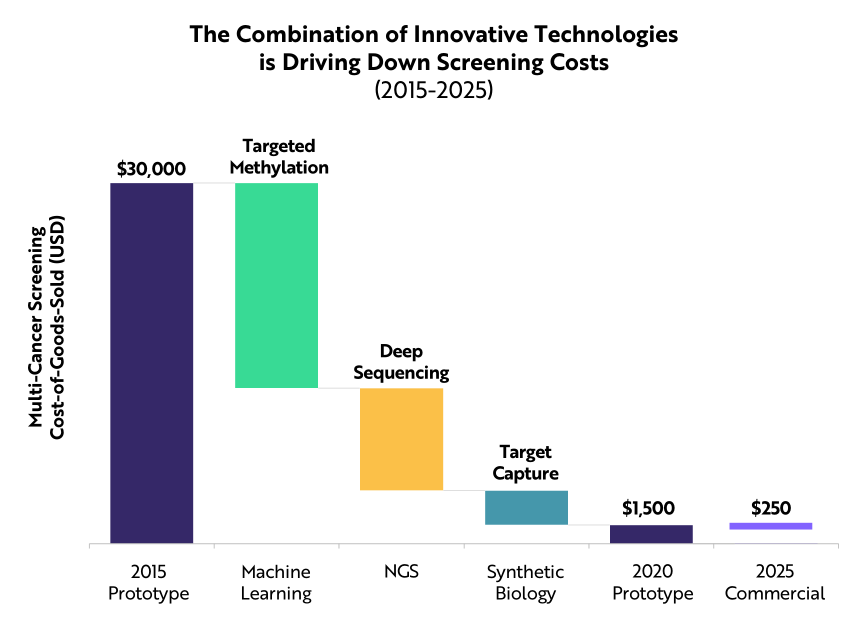
得益於成本迅速下降,多種癌症篩查價格正逐步接近可報銷範圍
隨著人口規模臨床實用數據的激增, ARK 認為, 1,500 美元的篩查對於 65 歲至 80 歲人群來說,剛好可以全額報銷, 65~80 歲的多癌篩查市場就此打開。值得注意的是,這些人群正處於癌症發病率最高的年齡段。隨著篩查價格跌破 1,000 美元,幾乎所有 40 歲以上的人群全額報銷癌症篩查的費用,僅在美國就能挽救高達 140 萬生命。
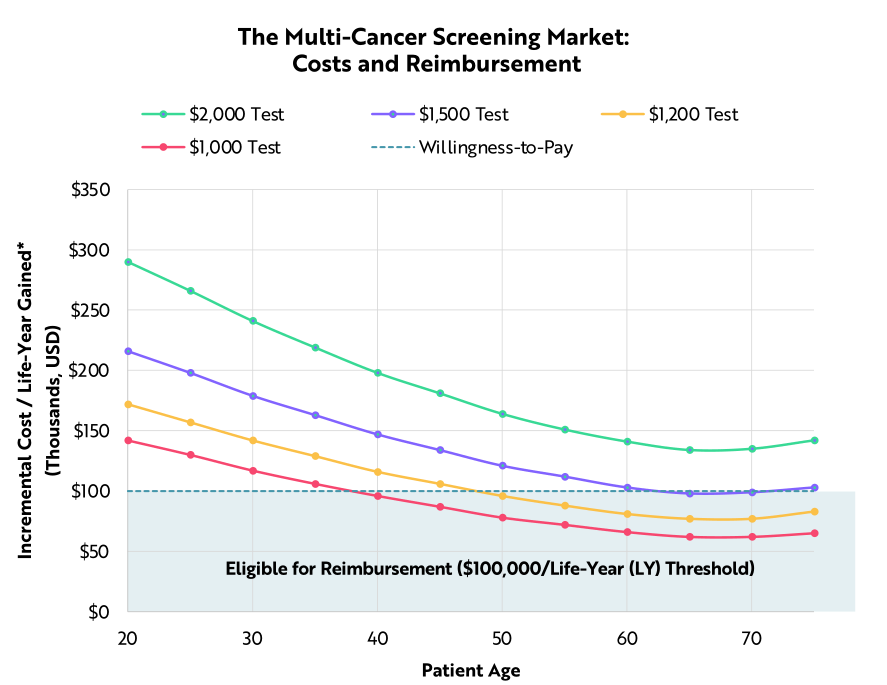
美國多癌症篩查每年可以預防大約 66,000 例癌症死亡
通過血液進行多癌症篩查,輔以單癌篩查的發展,轉移癌病例能夠下降 40% ,原位癌診斷發現病例提升 10% 。即使癌症治療方法未能有所突破, ARK 估計,僅在美國,早期干預每年就可以預防 66,000 例癌症死亡病例。
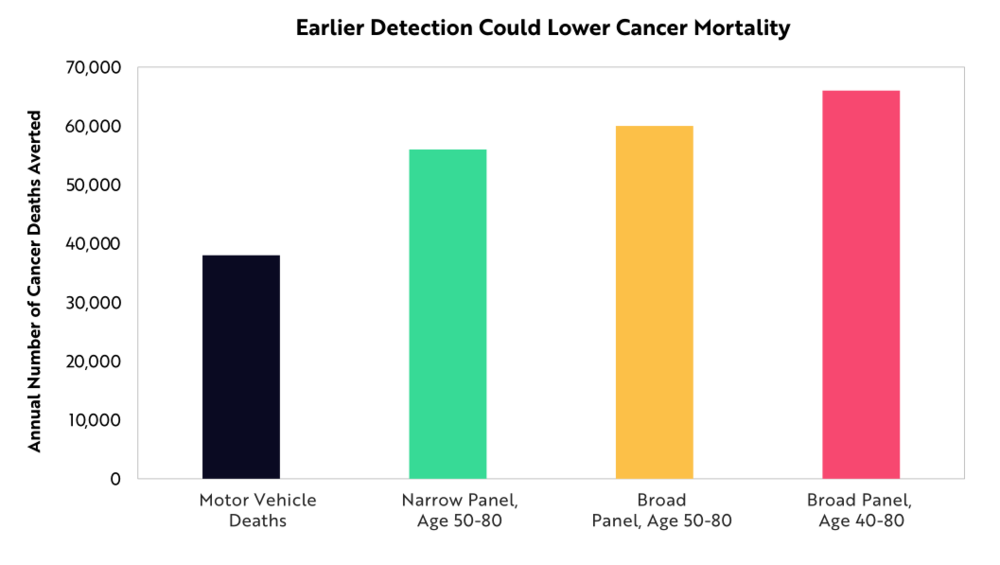
多種癌症篩查和其他基因組技術正為腫瘤學帶來變革
遺傳性癌症檢測可以影響癌症的發生和癌症篩查的頻率。多癌症篩查可以在早期和可治療階段排查癌症,同時單癌症篩查在檢測多種癌症方面起著至關重要的作用。分子預後測試可以幫助病理學家區分侵襲性和惰性癌症,減少過度治療。體細胞和微小殘留病變檢測能幫助腫瘤學家優化手術方案,確定精確的治療方法,並監測癌症的複發狀況。
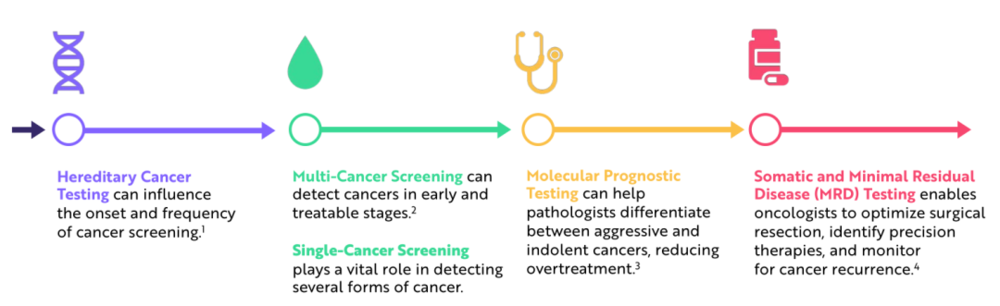
1,500 美元的篩查可以打開市場, 1,000 美元的篩查可以改變癌症死亡率曲線
綜合運用創新技術將多種癌症篩查的費用從 2015 年的 3 萬美元降到了現在的 1,500 美元,降低了 20 倍,根據 ARK 的研究, 2025 年的費用將再降低 80% ,達到 250 美元。如果多癌症篩查完全得到應用,那麼僅在美國,多癌症篩查市場規模就將擴大到 1,500 億美元。
第二代細胞和基因療法
細胞和基因療法尚處於早期階段第二代細胞和基因療法應當會發生轉變
從液體腫瘤轉向實體腫瘤,從自體細胞療法轉向異體細胞療法,從體外基因編輯轉向體內基因編輯,新的細胞和基因療法創新將使腫瘤治療的潛在目標市場增加 20 倍以上。
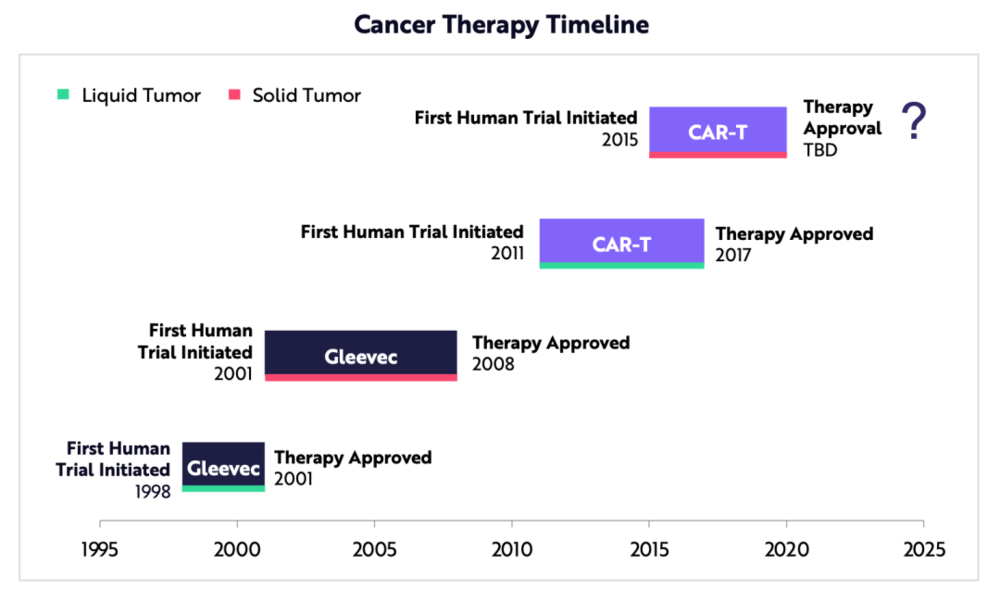
癌症治療正從液體腫瘤轉向實體腫瘤
通常,癌症療法首先在液體腫瘤上進行測試。然而,實體腫瘤佔確診癌症的 88% 。美國食品和藥物管理局( FDA )經過 10 年試驗後批准了口服化療藥格列衛 Gleevec ,其中 7 年用於實體腫瘤。這表明, FDA 可能會在 2025 年批准首個用於實體腫瘤的CAR-T療法。隨著人工智慧( AI )、基因編輯和下一代測序( NGS )技術的發展,實體腫瘤療法的失敗率將會下降,上市時間會縮短,從而加快其批准率。
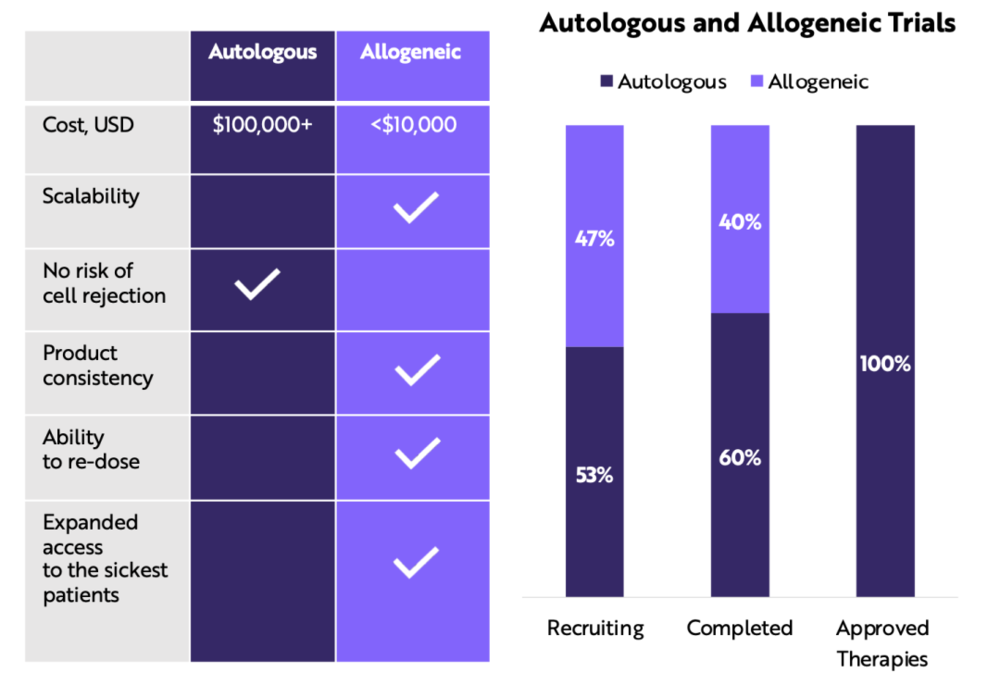
腫瘤學試驗正從自體細胞療法轉向異體細胞療法
異體細胞療法涉及現成的( off the shelf )或捐贈的細胞,而自體細胞療法則改變患者自身的細胞。
異體療法的風險之一是移植物抗宿主病( graft versus host disease, GVHD ),導致患者的免疫系統攻擊移植後異體供者移植物中的免疫細胞。儘管存在這種風險,異體細胞可以促進癌症早期治療,並將成本降低一個數量級。在當今基因治療試驗中,已完成的 40% 和處於患者招募階段的 47% 是異體基因。在 ARK 看來,向異體基因試驗的轉向將繼續下去。
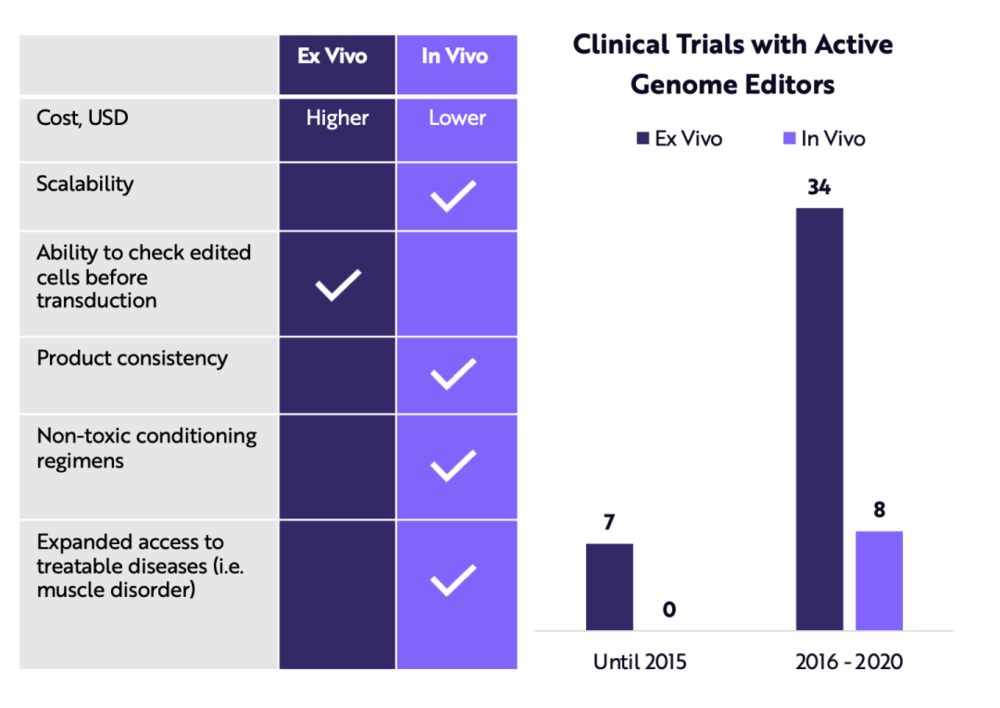
基因療法可能從體外編輯轉向體內編輯
體外療法在患者體外改變其細胞,然後將其移植回患者體內。體內基因療法則在患者體內改變其細胞。與體外療法不同,體內療法不能在細胞轉導前檢查編輯的細胞。也就是說,體內基因治療更具成本效益,更容易規模化。它還能廣泛應用於肝臟、眼睛、中樞神經系統( CNS )和肌肉。
自 2010 年以來,基因治療和編輯試驗增加了五倍
到目前為止, FDA 只批准了 10 種基因療法。截至 2020 年底, 712 項活性基因治療臨床試驗正在進行中,其中 238 項於 2020 年啟動。根據典型的試驗失敗率估算,大約有 170 種基因療法可能會在未來十年內獲得批准並商業化。
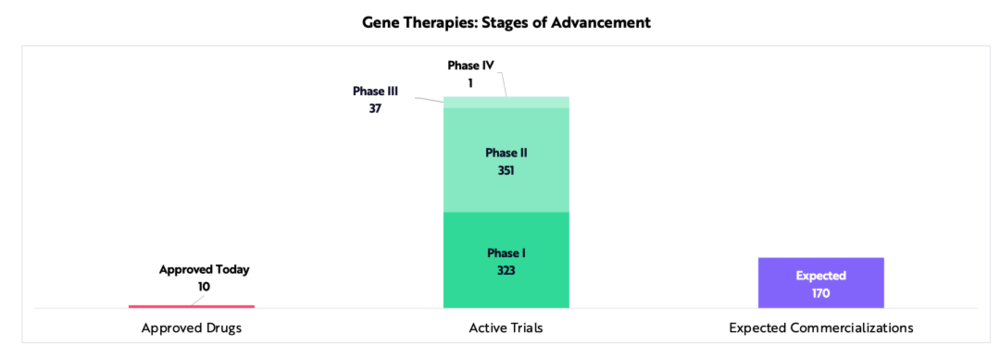
ARK 估計,異體細胞免疫療法可創造 2500 億美元的增量收入
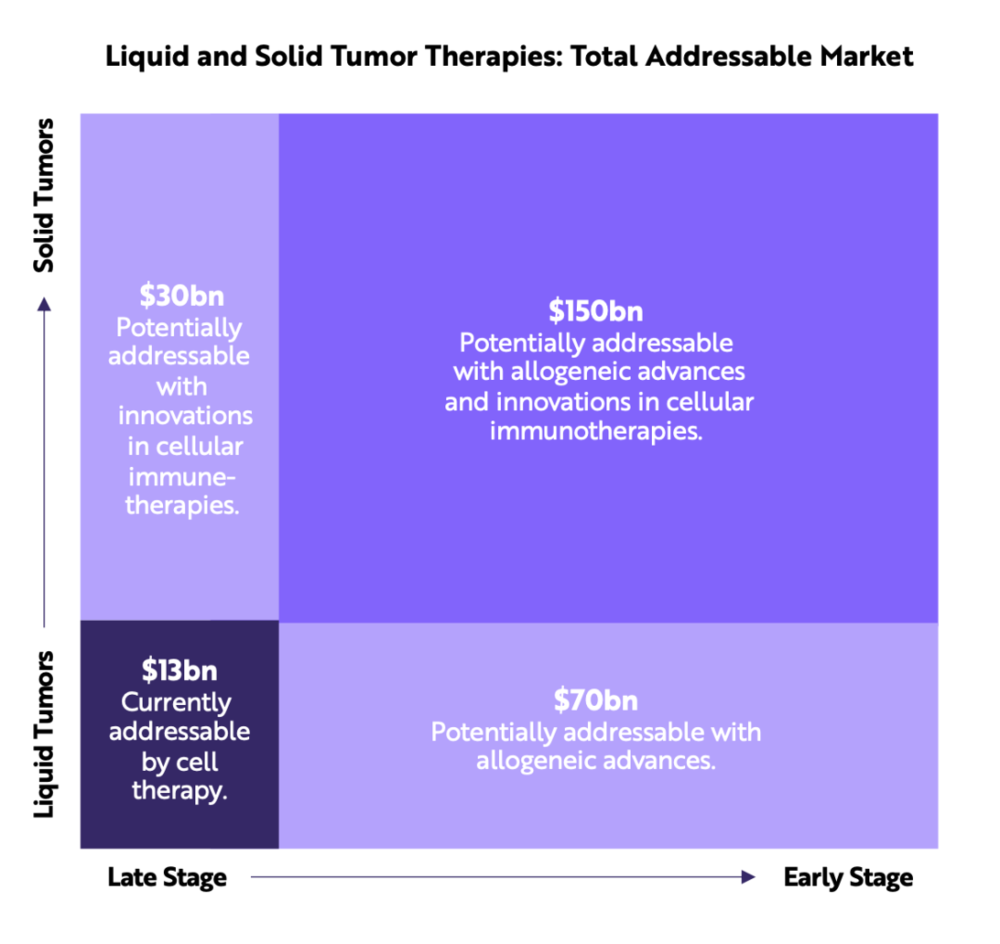
包括 TILs 、 TCRs 和 CAR-T 細胞療法在內的細胞免疫療法的創新,可以將潛在目標市場擴大近三倍,在目前 130 億美元的潛在目標市場( total addressable m ARK et,TAM )的基礎上增加 300 億美元。
異體療法在癌症早期應用更加容易,可能使TAM增加 700 億美元。細胞治療創新和異體細胞的結合可以額外增加 1,500 億美元,並將腫瘤基因治療的總 TAM 增加約 20 倍,達 2,600 億美元以上。隨著時間的推移,體內基因治療可以使基因編輯治癒數千種罕見的疾病。
《虎嗅網》授權轉載
【延伸閱讀】







全球CMOS影像感測器的領導廠商.png)