電池的構造與原理
所有的電池都具有陽極(負極)與陰極(正極),基本上都是由陽極(Anode)發生的化學反應產生電子(Electron)與陽離子(Ion),電子流入元件可以推動元件工作,也就是我們所稱的電能,如<圖一(a)>所示;陽離子則經由電解液穿越多孔性的隔離膜到達陰極,如<圖一(b)>所示;最後陽離子與電子在陰極(Cathode)結合,如<圖一(c)>所示。
電解液主要的功能是用來傳導陽離子,通常都是強酸或強鹼;隔離膜通常使用尼龍或聚丙烯(PP)不織布,必須具有許多孔隙讓陽離子流動,而且必須能夠抵抗強酸或強鹼電解液的腐蝕,並且能夠吸附電解液,同時具有絕緣性以防止陽極與陰極漏電短路。
此外,實際上電池可以依照不同的需要而製作成不同的形狀,可以製作成圓筒狀,例如:碳鋅電池、鹼性電池等,如<圖一(d)>所示,也可以製作為鈕扣狀,例如:汞電池(水銀電池)、銀電池等。
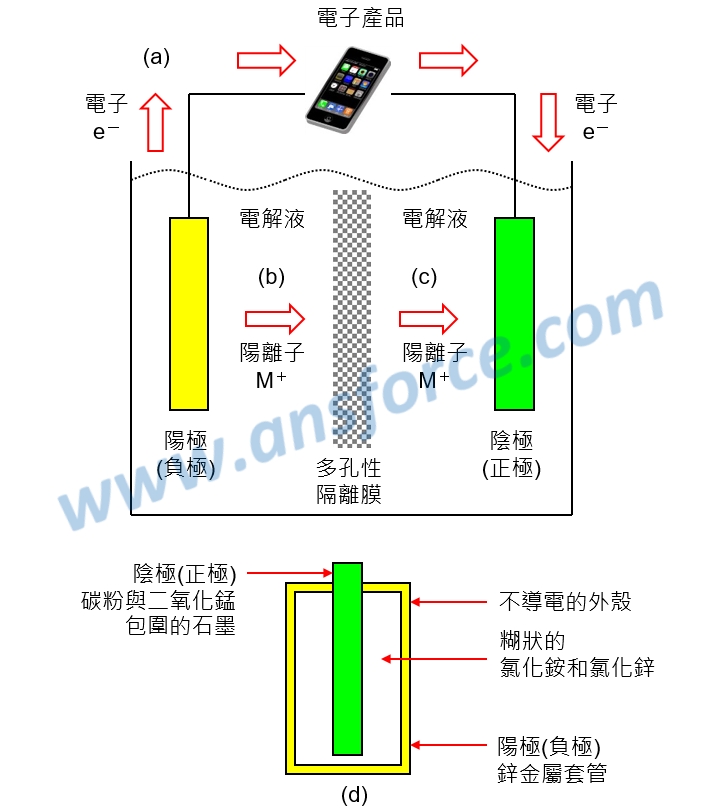
圖一、電池的構造
【重要觀念】
➤電池的陽極(Anode):是我們所稱的「負極(Negative electrode)」。
➤電池的陰極(Cathode):是我們所稱的「正極(Positive electrode)」。
兩者恰好相反,千萬別弄錯了唷!大家可能會好奇,為什麼會恰好相反來造成大家的困擾呢?因為化學家定義放出電子的叫「陽極」;而陽極放出電子,代表陽極必定帶負電(同性相斥、異性相吸),所以物理學家稱陽極為「負極」。
電池的能量密度
不同的電池其實只是陽極與陰極的材料不同、電解液不同,所以化學反應不同,產生的能量密度不同而已。能量密度的單位有兩種:
➤質量能量密度(Whr/Kg):是指電池每公斤(Kg)可以產生多少能量(瓦特 – 小時),質量能量密度愈高,代表相同質量的電池可以產生更多的電能。
➤體積能量密度(Whr/L):是指電池每公升(L)可以產生多少能量(瓦特 – 小時),體積能量密度愈高,代表相同體積的電池可以產生更多的電能。
記憶效應
電池的記憶效應,主要是由於電池充電或放電不完全,造成陽極材料(例如:鎳鎘電池的陽極為多晶鎘金屬)慢慢地產生較大的結晶,使得化學反應特性變差,能量密度變小。
➤充電不完全:是指電還沒充飽就停止充電,例如:使用者只充電到 60% 時就停止充電,如<圖二(a)>所示,則下一次再充電時,這個電池就只能充電到 60%,就好像電池記得上回使用者只充電到 60% 一樣,認定 60% 就是充滿了,所以這回也只充電到 60%。
➤放電不完全:是指電還沒用完就進行充電,例如:使用者只放電到 20% 時就停止放電,如<圖二(b)>所示,則下一次再放電時,這個電池就只能放電到 20%,就好像電池記得上回使用者只放電到 20% 一樣,認定 20% 就是放完了,所以這回也只放電到 20%。
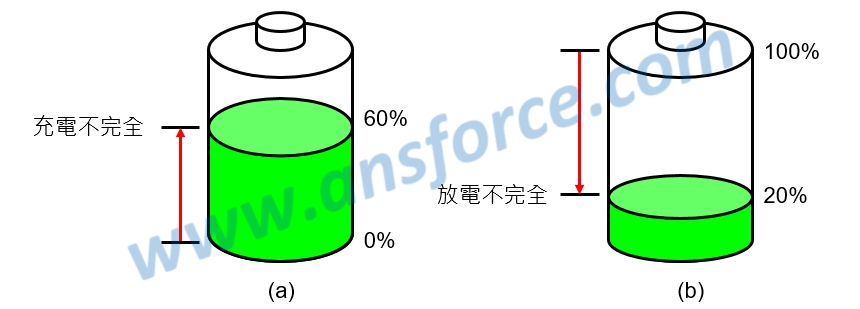
圖二、電池的記憶效應
記憶效應會造成陰極材料的化學反應特性變差,使電池暫時性的容量變小,通常只會發生在鎳鎘電池;鎳氫電池的記憶效應比較小,鋰電池的記憶效應更小。
避免記憶效應的方法是保持電池「用完再充、充滿再用」,可以使用具有放電功能的充電器,先進行放電後再充電,並且等充滿電能以後再使用;但是要記得,鋰電池的特性與鎳鎘電池、鎳氫電池不同,鋰電池幾乎沒有記憶效應,過度放電反而會造成電池損壞,因此不適合用完再充,一般用到 10% 以下就應該充電了!
自放電效應
電池的自放電效應,是指電池在充滿電能之後,如果沒有立刻使用,則電池內的化學物質仍然會產生化學反應,造成儲存的電能慢慢減少,在所有的二次電池中,自放電效應最嚴重的是鉛蓄電池與鎳鎘電池,最輕微的是鋰電池。
電池的分類
常見的電池可以分為一次電池與二次電池兩大類,如<圖三>所示:
➤一次電池:只能使用一次就必須丟棄,無法進行充電。
➤二次電池:可以進行充電而重覆使用,不過通常充電的次數會有限制,並不能永久使用,例如:第一次可以充電到 100%,但是第二次只能充電到 99%,充電的次數愈多則愈無法完全充飽,當充電次數多到某一個程度,就無法使用了。不同的二次電池會有不同的使用壽命,是我們選擇二次電池時必須參考的特性。
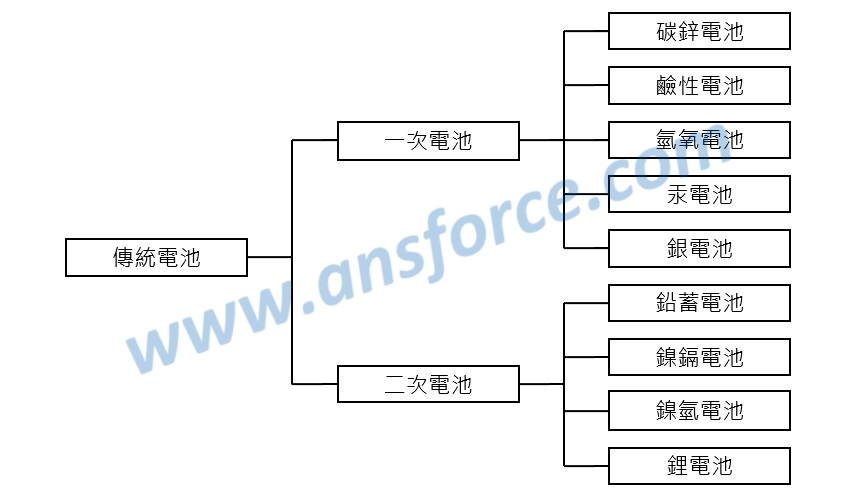
圖三、電池的分類
一次電池
➤碳鋅電池:陽極使用鋅(Zn)放出電子,陰極使用二氧化錳(MnO2)包覆碳棒(石墨),電解液為氯化銨水溶液。碳鋅電池的價格便宜、製造簡單,但是不適合大電流連續放電,而且放電電壓不穩定。
➤鹼性電池:陽極使用鋅放出電子,陰極使用二氧化錳,電解液為氫氧化鉀水溶液,由於氫氧化鉀是一種鹼性物質,故稱為「鹼性電池」。鹼性電池的放電電流較大、放電電壓穩定,但是價格較高。
➤氫氧電池:陽極使用鋅放出電子,陰極使用二氧化錳與氫氧化鎳(NiOH)包覆碳棒,電解液為氯化銨與氯化鋅水溶液。氫氧電池的能量密度是鹼性電池的二倍,也是目前能量密度最高的一次電池,但是價格較高因此沒有被大量使用。
➤汞電池(水銀電池):陽極使用鋅放出電子,陰極使用氧化汞及碳粉混合物,電解液為氧化鋅與氫氧化鉀水溶液。汞電池體積小、能量密度高、放電電壓穩定,常用於電子計算機、電子錶,而且價格較低,但是使用後丟棄,電池內的汞會造成環境污染。
➤銀電池:陽極使用鋅放出電子,陰極使用氧化銀及碳粉混合物,電解液為氧化鋅與氫氧化鉀水溶液。銀電池體積小、能量密度高、放電電壓穩定,常用於電子計算機、電子錶,但是價格較高。
二次電池
➤鉛蓄電池:陽極使用鉛(Pb)放出電子,陰極使用氧化鉛(PbO2),電解液為硫酸水溶液,由於硫酸是一種酸性物質,故又稱為「鉛酸電池」。鉛蓄電池是第一個商業化與最廣泛使用的二次電池,結構簡單、重覆使用壽命長、操作溫度範圍大、價格便宜,但是體積龐大、重量較重、不易攜帶,主要使用在汽車電池,通氣式的鉛蓄電池需要定期加水補充水分的蒸發,最近幾年已經有密閉式的鉛蓄電池出現,不需要加水補充比較方便。
➤鎳鎘電池:陽極使用鎘(Cd)放出電子,陰極使用二氧化鎳,電解液為鹼性液體。鎳鎘電池體積小,原本是使用量最大的二次電池,曾經廣泛的應用在各種電子產品,但是使用後丟棄,電池內的鎘會造成環境污染,而且記憶效應較大,目前已經禁止使用了。
➤鎳氫電池:陽極使用氫氧化鎳放出電子,陰極使用儲氫合金吸收電子同時放出氫原子,電解液為鹼性液體。鎳氫電池的能量密度是鎳鎘電池的二倍,組成材料與鎳鎘電池相似,由於不含鎘比較不會造成環境污染,而且記憶效應較小,所以目前已經取代鎳鎘電池廣泛的應用在各種電子產品。如何增加能量密度必須改良儲氫合金,由於儲氫合金是所有必須使用氫能的電池都要使用的技術,是氫能產業重要的技術,請參考<燃料電池>的詳細介紹。
➤鋰電池:陽極將鋰離子嵌在石墨結構中,陰極使用鋰鈷氧化物(LiCoO2)、鋰鎳氧化物(LiNiO2)或鋰錳氧化物(LiMn2O4),電解液為鋰離子化合物有機溶液,後面會再特別針對鋰電池詳細介紹。
常見的二次電池比較如<表一>所示,其中鋰電池的質量能量密度最高,但是價格也最高,而且由於鋰的活性很高,遇到水很容易將水分解產生氫氣,尤其是空氣裡原本就含有水份,所以比較容易爆炸,使用時要非常小心。
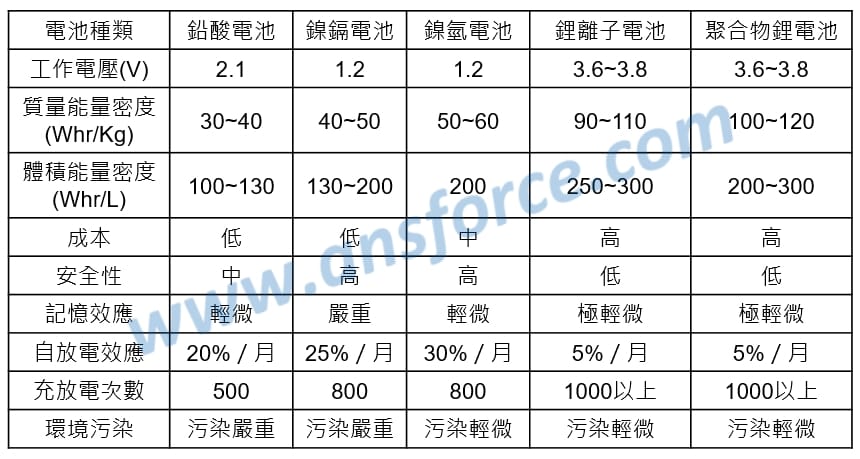
表一、常見的二次電池比較表(資料來源:Electronics Lab website、國科會)
【請注意】上述內容經過適當簡化以適合大眾閱讀,與產業現狀可能會有差異,若您是這個領域的專家想要提供意見,請自行聯絡作者;若有產業與技術問題請參與社群討論。
《知識力》授權轉載
【延伸閱讀】









margin-of-safety_-.png)